Separação fotocatalítica da água
O hidrogênio é um combustível limpo por excelência, podendo gerar diretamente eletricidade em células a combustível ou ser simplesmente queimado – sempre liberando apenas água como subproduto.
O problema é que a maior parte do hidrogênio hoje é produzido pela reforma do gás natural, deixando pegadas bem sujas atrás de si.
O hidrogênio solar e a fotossíntese artificial estão a caminho, ambas usando energia solar para fazer eletrólise da água, mas ainda não conseguem suprir nossas enormes demandas energéticas.
Agora, uma nova rota para obter o hidrogênio verde acaba de ser criada pelas equipes dos professores Alexey Cherevan e Dominik Eder, da Universidade de Tecnologia de Viena, na Áustria.
O novo processo chama-se “separação fotocatalítica da água”. O termo “foto” aponta para o uso de luz – e pode ser a luz do Sol – para ativar catalisadores de baixo custo que quebram as moléculas de água, separando-as em hidrogênio e oxigênio.
Embora tudo tenha sido demonstrado apenas em escala laboratorial, a equipe não vê entraves fundamentais para que a tecnologia seja escalonada para operar em larga escala.
Rota do oxigênio e rota do hidrogênio
“Na verdade, para poder dividir a água usando luz, você precisa resolver duas tarefas ao mesmo tempo,” explica o professor Cherevan. “Temos que pensar no oxigênio e no hidrogênio. Os átomos de oxigênio da água devem ser transformados em moléculas de O2, e os íons de hidrogênio restantes – que são apenas prótons – devem ser transformados em moléculas de H2.”
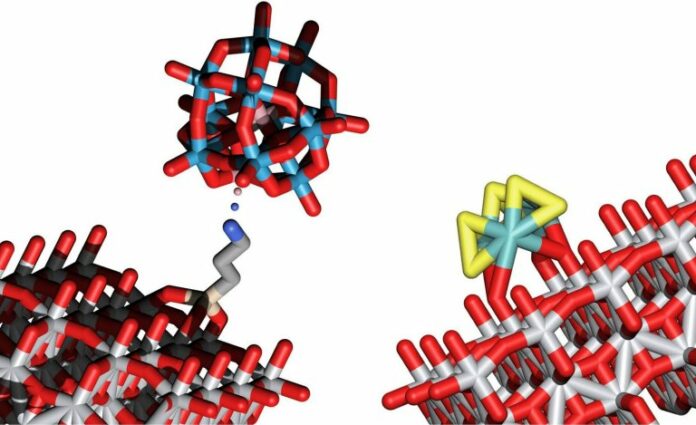
A solução encontrada pela equipe faz as duas coisas: Nanopartículas inorgânicas, formadas por apenas alguns átomos, são ancoradas em uma superfície de suporte contendo materiais absorvedores de luz, como o óxido de titânio.
O grande feito da equipe foi pacientemente obter a combinação precisa desses aglomerados e dos suportes semicondutores para obter exatamente o comportamento desejado: Entra água e luz e saem moléculas de oxigênio e hidrogênio. As nanopartículas responsáveis pela oxidação do oxigênio são compostas de cobalto, tungstênio e oxigênio, enquanto nanopartículas de enxofre e molibdênio mostraram-se especialmente adequadas para a criação de moléculas de hidrogênio.
“O óxido de titânio é sensível à luz, isso já era bem conhecido,” disse Cherevan. “A energia da luz absorvida leva à criação de elétrons livres e cargas positivas livres no óxido de titânio. Essas cargas então permitem que os aglomerados de átomos assentados nesta superfície facilitem a divisão da água em oxigênio e hidrogênio.”
Agora que foi comprovado que os materiais selecionados são realmente adequados para dividir a água, o próximo passo será ajustar ainda mais a estrutura exata para obter eficiências ainda maiores.
A longo prazo, segundo a equipe, o processo que eles desenvolveram também poderá vir a ser usado para produzir moléculas mais complicadas usando o conceito de fotossíntese artificial. Pode até ser possível usar a energia da radiação solar para produzir hidrocarbonetos usando dióxido de carbono da atmosfera e água, que podem ser usados para outras aplicações.
Artigo: Surface Anchoring and Active Sites of [Mo3S13]2- Clusters as Co-Catalysts for Photocatalytic Hydrogen Evolution
Autores: Samar Batool, Sreejith P. Nandan, Stephen Nagaraju Myakala, Ashwene Rajagopal, Jasmin S. Schubert, Pablo Ayala, Shaghayegh Naghdi, Hikaru Saito, Johannes Bernardi, Carsten Streb, Alexey Cherevan, Dominik Eder
Revista: Catalysis
DOI: 10.1021/acscatal.2c00972
Artigo: Immobilization of a [CoIIICoII(H2O)W11O39]7- Polyoxoanion for the Photocatalytic Oxygen Evolution Reaction
Autores: Sreejith P. Nandan, Nadiia I. Gumerova, Jasmin S. Schubert, Hikaru Saito, Annette Rompel, Alexey Cherevan, Dominik Eder
Revista: Catalysis
DOI: 10.1021/acsmaterialsau.2c00025





